UdeC integra alianza científica traslacional para enfrentar el problema del dolor crónico
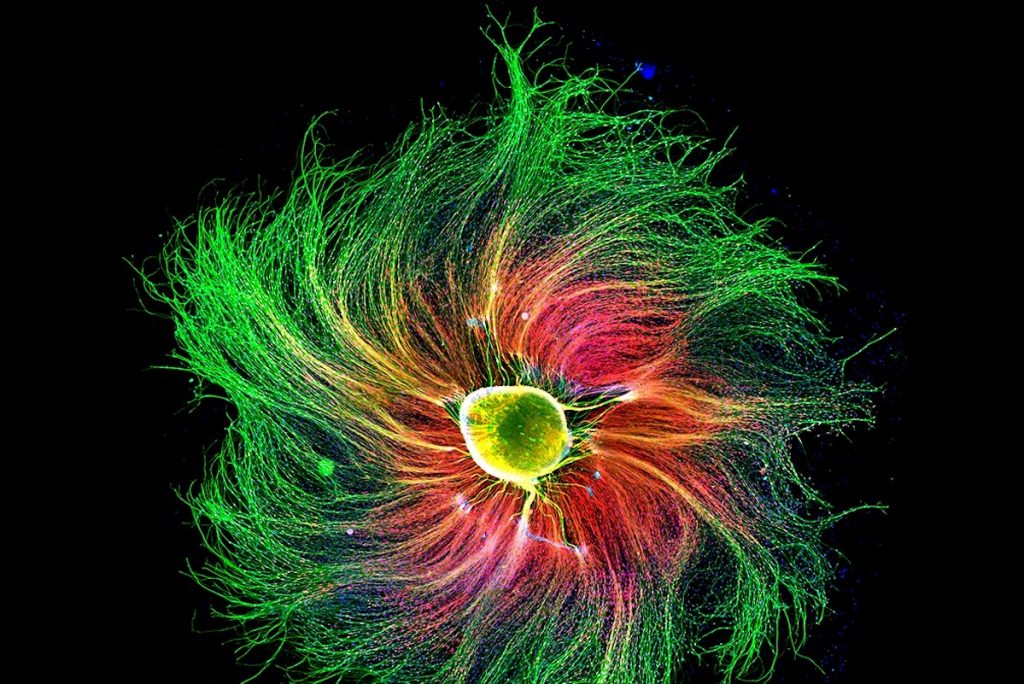
Crédito: Facultad de Ciencias Biológicas.
El dolor neuropático genera consecuencias físicas, psíquicas, sociales y laborales incapacitantes y es de alta prevalencia. Los medicamentos actuales son poco eficaces, por lo que el desarrollo de investigación para entender los mecanismos del dolor y generar nuevas terapias, es fundamental.
Intenso y debilitante, quemante y con sensaciones desagradables agregadas. Así describe la Dra. Margarita Calvo la forma en que los pacientes perciben el dolor neuropático.
“Es paroxístico, es decir que aparece sin previo aviso y generalmente provoca temor de que esto les ocurra repentinamente, por esto los pacientes comienzan a evitar algunas actividades de su vida cotidiana, con severas consecuencias psíquicas, emocionales, sociales y laborales”, detalla.
La académica de la Pontificia Universidad Católica (PUC), asumió recientemente la dirección del Núcleo Milenio para el Estudio del Dolor, MiNuSPain, uno de los cinco nuevos centros de este tipo financiados por la Iniciativa Científica Milenio de la Agencia Nacional de Investigación y Desarrollo (ANID) a partir de este año.
Se trata de un consorcio que reúne a investigadores de las universidades Pontificia Católica de Chile, de Concepción, de Santiago de Chile, Católica del Norte y de Chile, en un esfuerzo traslacional por encontrar nuevas alternativas terapéuticas que puedan ser relevantes para el dolor neuropático.
La especialista ha estudiado por más de 15 años los mecanismos moleculares y celulares que provocan el dolor neuropático, alteración causada por una enfermedad que afecta el sistema nervioso somatosensorial, dañando las fibras nerviosas donde se alojan los receptores del dolor y alterando la precepción. Esto provoca que el paciente tenga una sensación incrementada frente a estímulos dolorosos y más aún frente a otros que no deberían causarlo, como el simple roce de una sábana.
Se trata de una patología de alta prevalencia que afecta entre un 7 a un 10% de la población y, a pesar de ello, es de difícil diagnóstico y de aún más complejo tratamiento. “De cada seis pacientes tratados con los fármacos disponibles, sólo uno logra resultados, pero ese resultado se traduce en que su dolor va a disminuir sólo en un 30%. Esa falta de eficacia, sumado a que tienen una larga lista de efectos adversos, hace que muchos pacientes abandonen los tratamientos”, expuso la Dra. Calvo.
Las consecuencias de ello son devastadoras para quien lo sufre, “sin opciones de tratamiento, estos pacientes quedan con un dolor muy severo e incapacitante que, además, es poco entendido por su entorno, porque la causa no es una lesión visible, sino que es un daño en la fibra nerviosa que no se observa a simple vista”, expuso la académica.
MiNuSPain apuesta a encontrar nuevas opciones terapéuticas que permitan mejorar la calidad de vida de miles de personas afectadas por este problema.
“Somos cinco grupos de científicos que colaborativamente abordamos el estudio de las vías de señalización del dolor desde distintas perspectivas, tanto a nivel de sistema nervioso periférico, como a nivel central”, explicó el Dr. Elías Utreras, Director Alterno del Centro y académico de la Universidad de Chile.
El investigador planteó que el mundo científico aún desconoce los mecanismos exactos por los cuales se percibe el dolor, en un proceso que inicia con la activación de los receptores que se encuentran en las terminales nerviosas y que luego son transformados en impulsos eléctricos que viajan a través del sistema nervioso periférico, hasta la médula espinal y el cerebro, donde finalmente es interpretado, en un recorrido que dura apenas algunas décimas de segundo. Las alteraciones de esta secuencia, sin embargo, pueden ser catastróficas para el paciente.
“Integrar estas visiones para el estudio a nivel molecular del dolor, con las distintas aproximaciones experimentales que tenemos en el equipo, es importante para tratar de entender este proceso a cabalidad e identificar nuevos blancos moleculares clínicamente relevantes que podrían estar participando”, enfatizó el docente de la casa de Bello.
Al respecto, el académico de la Universidad de Concepción e investigador asociado del Núcleo Milenio MiNuSPain, Dr. Gonzalo Yévenes, expuso que una de las ventajas de la plataforma de trabajo propuesta por el Núcleo Milenio MiNuSPain es la integración entre ciencia biomédica y clínica a través de un abordaje denominado “bedsite to bench and back”.
“Nuestro proyecto integra la investigación preclínica con la investigación clínica, la combinación ideal; eso nos podría llevar a entender de mejor manera los procesos. Pero, a la vez, nos permitirá generar nuevos blancos farmacológicos, tanto en la neurona sensorial como en el sistema nervioso central, ya sea la médula espinal o, incluso, a nivel del cerebro”, afirmó. Con ello, aseguró, se amplían las posibilidades de encontrar nuevos tratamientos que mejoren la eficacia de los actuales.
Diversos tipos de dolor
En el caso de la línea de trabajo desarrollada por el laboratorio en la Universidad de Concepción, el estudio está enfocado en los receptores de glicina, una subclase de receptores inhibitorios del sistema nervioso central presentes en la médula espinal, que constituye la primera estación de procesamiento de los estímulos de dolor que vienen desde la periferia.
“Nuestra investigación ha mostrado que este tipo de receptor es muy promisorio para desarrollar nuevos analgésicos que tengan, en este caso, un blanco muy poco explorado en el área del control del dolor”, argumentó el Dr. Gonzalo Yévenes.
Otra línea de trabajo se desarrolla en los laboratorios de la Universidad de Santiago de Chile, a cargo del investigador asociado del Núcleo Milenio MiNuSPain y del Núcleo Milenio MiNICAD, Dr. Rodolfo Madrid, quien aborda el daño nervioso periférico asociado a la córnea en una de sus líneas de investigación.
“La córnea es el tejido más densamente inervado del cuerpo. En situaciones de daño en la superficie ocular causado, por ejemplo, en las cirugías correctivas o por el uso constante de lentes de contacto u otras formas de daño traumático que impliquen el deterioro de las neuronas sensoriales que inervan la córnea, se pueden producir alteraciones tanto en la morfología de las terminales, como en los niveles de expresión funcional de algunos canales de iones relevantes para su respuesta a estímulos”, explicó el académico.
Agregó que “las múltiples alteraciones funcionales que sufren los diferentes tipos de neuronas trigeminales que inervan la córnea tras el daño axonal, pueden a largo plazo transformarse en una fuente de dolor neuropático”.
“En nuestro laboratorio estudiamos el papel que tienen en estas alteraciones los canales de iones de la superfamilia TRP, entre otros, no sólo en este tejido, sino en diversos territorios somáticos”, explicó.
De esta forma, el investigador de la Usach busca encontrar nuevas dianas moleculares y neurales que permitan corregir estas alteraciones y combatir el dolor neuropático asociado al daño axonal periférico.
En tanto, el trabajo liderado por el académico de la Universidad Católica del Norte, Dr. Claudio Coddou, ha identificado a una proteína, el receptor purinérgico P2X3, que ya ha demostrado su efectividad como sedante y que podría ser clave para el desarrollo de nuevos fármacos.
“Se han realizado numerosos estudios en modelos preclínicos y se ha verificado su efecto analgésico y, actualmente, existen estudios similares para, al menos, 5 moléculas distintas que tienen efectos sobre receptores purinérgicos”,
El científico detalló que “del mismo modo, al estudiar otros procesos regulatorios de esta proteína, también se pueden elaborar estrategias más eficaces y selectivas que actúen sobre los subtipos de receptores específicos que tengan una mayor contribución en la señalización del dolor”. Es decir, se podrían generar blancos farmacológicos específicos para el control del dolor en diversas patologías.
Encontrar nuevas terapias que sean más efectivas es fundamental, dada la magnitud del problema en Chile. Se estima que cerca de 10% del presupuesto anual de salud del país se destina al gasto por concepto de atención médica del dolor, lo que es equivalente al total de recursos asignados para el desarrollo de ciencia en Chile.
“Invertir en el desarrollo de ciencia que permita mejorar la calidad de vida de miles de personas con dolor neuropático es no sólo una forma de evitar mayor gasto público a futuro, sino una responsabilidad social que permite entregar bienestar y calidad de vida a miles de pacientes y a sus entornos, quienes sufren a diario por este padecimiento”, puntualizó sobre este problema la directora del Núcleo Milenio MiNuSPain, Dra. Margarita Calvo.
- Compartir
- Compartir
Noticias relacionadas
Reportajes